ورم الخلايا العملاقة في العظم: دليل شامل للمرضى مع الأستاذ الدكتور محمد هطيف
الخلاصة الطبية
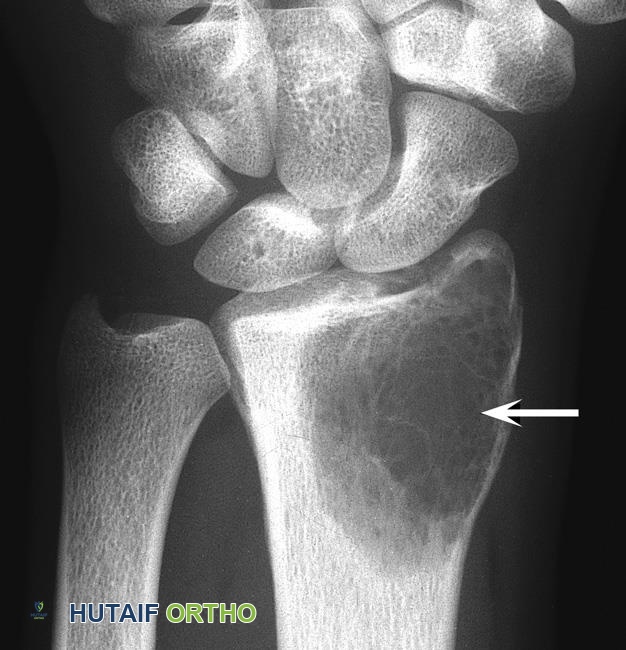
**ورم الخلايا العملاقة في العظم** هو ورم حميد، ولكنه يتميز بسلوك عدواني، وينمو غالبًا في نهايات العظام الطويلة قرب المفاصل. يتضمن علاجه بشكل أساسي الاستئصال الجراحي بالكي أو جراحة متقدمة للحفاظ على العظم والوظيفة، وقد تستخدم خيارات أخرى كالعلاج الإشعاعي أو الدوائي في حالات خاصة.
الخلاصة الطبية السريعة: ورم الخلايا العملاقة في العظم هو ورم حميد ولكنه عدواني، ينمو غالبًا في نهايات العظام الطويلة قرب المفاصل. يتضمن علاجه الأساسي الاستئصال الجراحي بالكي أو الاستئصال الأكثر تعقيدًا للحفاظ على العظم والوظيفة، وقد تشمل الخيارات الأخرى العلاج الإشعاعي أو الدوائي في حالات معينة. يؤكد الأستاذ الدكتور محمد هطيف، أحد أبرز استشاريي جراحة العظام والمفاصل في اليمن، على أهمية التشخيص الدقيق والعلاج المتخصص لضمان أفضل النتائج للمرضى.

مقدمة شاملة لورم الخلايا العملاقة
يعد ورم الخلايا العملاقة في العظم (Giant Cell Tumor of Bone - GCTB) أحد أنواع الأورام التي قد تصيب الهيكل العظمي، وعلى الرغم من أنه يوصف عادة بأنه ورم حميد (غير سرطاني)، إلا أنه يتميز بسلوك عدواني وقدرة على تدمير العظم المحيط به. يشكل فهم هذا الورم، من حيث طبيعته وأعراضه وتشخيصه وخيارات علاجه، حجر الزاوية في إدارة الحالة بنجاح. في هذا الدليل الشامل، نقدم للمرضى وأسرهم معلومات مفصلة وموثوقة حول ورم الخلايا العملاقة في العظم، مستندين إلى أحدث الممارسات الطبية والخبرة الواسعة للأستاذ الدكتور محمد هطيف، استشاري جراحة العظام والمفاصل، أستاذ جراحة العظام بجامعة صنعاء، والذي يتمتع بخبرة تزيد عن 20 عامًا في التعامل مع هذه الحالات المعقدة.
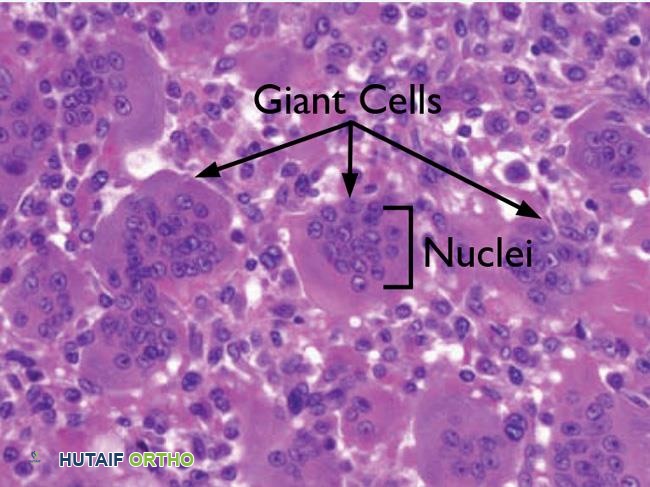
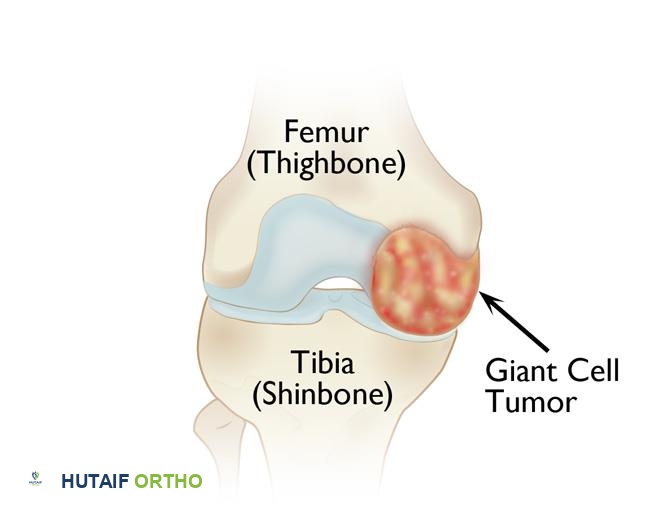
إن ورم الخلايا العملاقة هو ورم نادر نسبياً، يمثل حوالي 4-5% من جميع أورام العظام الأولية وحوالي 20% من أورام العظام الحميدة. يُصيب غالبًا الشباب في الفئة العمرية بين 20 و40 عامًا، ويُلاحظ بشكل متكرر في نهايات العظام الطويلة (epiphysis)، خاصة حول الركبة (عظم الفخذ السفلي وقصبة الساق العلوية) والرسغ (عظم الكعبرة السفلي). على الرغم من كونه حميدًا، إلا أن سلوكه العدواني يجعله تحديًا علاجيًا يتطلب نهجًا متخصصًا ودقيقًا لتجنب التدمير الموضعي للعظم والمفصل، وتقليل احتمالية تكرار الورم.
د محمد هطيف خبرة في أورام العظام
يُعرف الأستاذ الدكتور محمد هطيف بكونه مرجعية طبية في مجال جراحة العظام والمفاصل في اليمن. بفضل خبرته التي تتجاوز العقدين، وحرصه على تطبيق أحدث التقنيات العالمية مثل الجراحات المجهرية (Microsurgery)، ومناظير المفاصل بتقنية 4K (Arthroscopy 4K)، وجراحات استبدال المفاصل (Arthroplasty)، يقدم الدكتور هطيف رعاية شاملة ومتطورة لمرضاه. إن التزامه بالصدق الطبي والشفافية مع المرضى يجعله الخيار الأول للعديد من الحالات المعقدة، بما في ذلك ورم الخلايا العملاقة في العظم، حيث يضمن حصول المريض على التشخيص الأدق والعلاج الأمثل القائم على الأدلة العلمية.
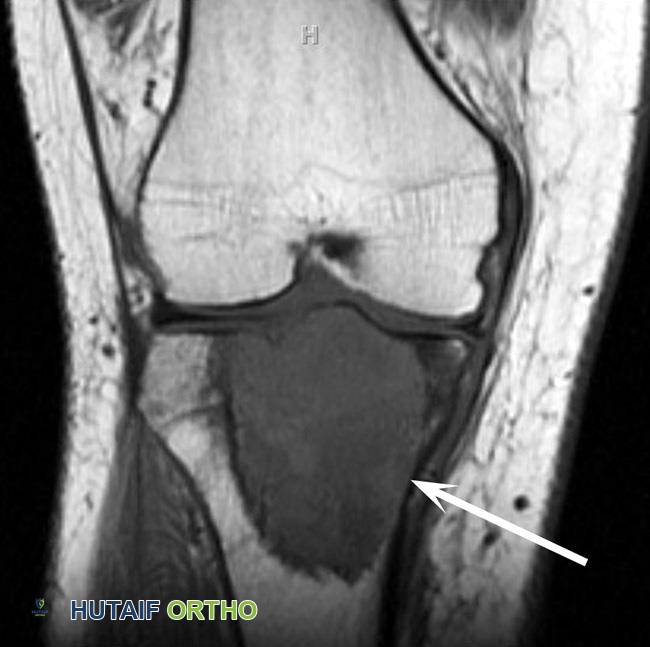
فهم ورم الخلايا العملاقة في العظم علم التشريح والفيزيولوجيا
لفهم ورم الخلايا العملاقة في العظم بشكل أفضل، من المهم التعرف على طبيعته التشريحية وكيفية تطوره على المستوى الخلوي.
أين ينمو ورم الخلايا العملاقة عادة
يُفضل ورم الخلايا العملاقة النمو في منطقة "الفيزيولوجيا" أو "المشاشة" (epiphysis) للعظام الطويلة، وهي المنطقة القريبة من المفاصل. العظام الأكثر شيوعًا للإصابة تشمل:
* عظم الفخذ السفلي (distal femur): فوق الركبة.
* قصبة الساق العلوية (proximal tibia): تحت الركبة.
* عظم الكعبرة السفلي (distal radius): عند الرسغ.
* يمكن أن يصيب أيضًا عظامًا أخرى مثل العمود الفقري والحوض، وإن كان ذلك أقل شيوعًا.
ما الذي يتكون منه الورم
يتكون ورم الخلايا العملاقة من نوعين رئيسيين من الخلايا:
1. الخلايا العملاقة متعددة النوى (multinucleated giant cells): وهي خلايا كبيرة تحتوي على العديد من الأنوية، وتشبه خلايا ناقضات العظم (osteoclasts) المسؤولة عن تآكل العظم الطبيعي. هذه الخلايا هي التي تعطي الورم اسمه.
2. الخلايا أحادية النواة السدوية (mononuclear stromal cells): يُعتقد أن هذه الخلايا هي المكون الأساسي للورم وهي المسؤولة عن سلوكه العدواني. تنتج هذه الخلايا مواد كيميائية تحفز الخلايا العملاقة على تدمير العظم.
لماذا هو عدواني رغم كونه حميدا
على الرغم من أن ورم الخلايا العملاقة لا ينتشر عادةً إلى أجزاء أخرى من الجسم (نادرًا ما يحدث انتشار رئوي حميد)، إلا أنه يُظهر سلوكًا عدوانيًا محليًا:
* التدمير الموضعي للعظم: يتميز بقدرته على تآكل وتدمير العظم المحيط به، مما يؤدي إلى إضعاف العظم وزيادة خطر الكسور المرضية.
* ارتفاع معدل التكرار: بعد الاستئصال الجراحي، يمكن أن يعاود الورم الظهور في نفس الموقع (recurrence) بنسبة تتراوح بين 20-50% إذا لم يتم استئصاله بشكل كامل أو استخدام علاجات مساعدة.
* التأثير على المفصل: نظرًا لنموه القريب من المفاصل، يمكن أن يؤثر على وظيفة المفصل ويسبب تدميرًا للغضاريف المحيطة.
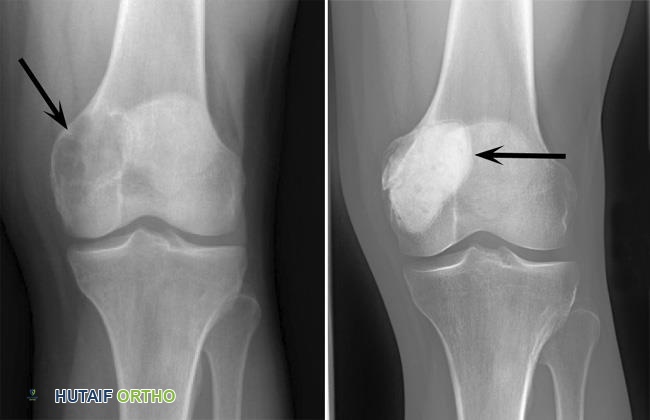
الأسباب وعوامل الخطر تحليل الأستاذ الدكتور هطيف
السبب الدقيق لورم الخلايا العملاقة في العظم لا يزال غير مفهوم تمامًا، ويُعتقد أنه ينشأ بشكل تلقائي في معظم الحالات. ومع ذلك، هناك بعض العوامل والآليات التي يُعتقد أنها تلعب دورًا في تطوره:
الآليات الخلوية والجزيئية
- مسار RANKL: أظهرت الأبحاث الحديثة أن مسار RANKL (Receptor Activator of Nuclear factor Kappa-B Ligand) يلعب دورًا حاسمًا في تطور ورم الخلايا العملاقة. تنتج الخلايا أحادية النواة في الورم كميات كبيرة من RANKL، والتي ترتبط بمستقبلات RANK على الخلايا العملاقة، مما يحفزها على التمايز والتنشيط، وبالتالي زيادة تآكل العظم. هذا الاكتشاف أدى إلى تطوير علاجات دوائية مستهدفة مثل دواء دينوسوماب (Denosumab).
- الطفرات الجينية: تم تحديد طفرة جينية في جين H3F3A في حوالي 90% من أورام الخلايا العملاقة، مما يشير إلى دور وراثي محتمل في بعض الحالات، على الرغم من أن الورم لا يُورث عادةً.
العوامل الديموغرافية
- العمر: يُصيب الورم بشكل أساسي الأفراد في الفئة العمرية الشابة، وعادة ما يكون بين 20 و40 عامًا. نادراً ما يُرى في الأطفال أو كبار السن.
- الجنس: يُلاحظ أن الورم أكثر شيوعًا بشكل طفيف لدى الإناث مقارنة بالذكور.
- العوامل البيئية: لا توجد أدلة قوية تربط ورم الخلايا العملاقة بعوامل بيئية محددة أو نمط حياة معين.
يؤكد الأستاذ الدكتور محمد هطيف أن فهم هذه الآليات يساعد في تطوير استراتيجيات علاجية أكثر فعالية، سواء جراحية أو دوائية، ويوجه الأبحاث المستقبلية نحو اكتشاف علاجات جديدة.
الأعراض والتشخيص نهج دقيق وشامل
تُعد الدقة في التشخيص حجر الزاوية في علاج ورم الخلايا العملاقة في العظم، وهذا ما يشدد عليه الأستاذ الدكتور محمد هطيف في ممارسته. الأعراض غالبًا ما تكون غير محددة في البداية، مما يجعل التشخيص المبكر تحديًا.
الأعراض الشائعة
تتطور أعراض ورم الخلايا العملاقة تدريجياً وتزداد سوءًا مع نمو الورم:
* الألم: هو العرض الأكثر شيوعًا. يكون الألم موضعيًا في المنطقة المصابة، وقد يكون خفيفًا في البداية ثم يزداد شدة مع مرور الوقت، وقد يتفاقم أثناء النشاط البدني أو في الليل.
* التورم: قد يلاحظ المريض تورمًا أو كتلة محسوسة حول المفصل المصاب، خاصة في المراحل المتقدمة.
* الحد من حركة المفصل: بسبب الألم أو التورم أو تدمير المفصل، قد يواجه المريض صعوبة في تحريك المفصل المصاب بشكل كامل.
* الكسور المرضية: نظرًا لقدرة الورم على تدمير العظم، يصبح العظم ضعيفًا وهشًا، مما يزيد من خطر حدوث كسور حتى مع إصابات طفيفة (كسر مرضي).
* الشعور بالدفء أو الاحمرار: في بعض الحالات، قد يكون هناك شعور بالدفء أو احمرار خفيف فوق منطقة الورم.
جدول 1: الأعراض الشائعة لورم الخلايا العملاقة في العظم
| العرض | الوصف | مدى الشيوع |
|---|---|---|
| الألم الموضعي | يبدأ خفيفًا ويزداد شدة، خاصة مع النشاط أو في الليل. | شائع جدًا |
| التورم | كتلة محسوسة أو انتفاخ حول المفصل المصاب. | شائع |
| الحد من حركة المفصل | صعوبة في تحريك المفصل المصاب بسبب الألم أو التورم. | شائع |
| الكسور المرضية | كسر يحدث في عظم ضعيف بسبب الورم، حتى مع إصابة بسيطة. | متوسط |
| الدفء أو الاحمرار | شعور بالدفء أو احمرار خفيف فوق المنطقة المصابة. | أقل شيوعًا |
عملية التشخيص الشاملة
يتبع الأستاذ الدكتور محمد هطيف نهجًا متعدد الخطوات لضمان تشخيص دقيق لورم الخلايا العملاقة:
-
التاريخ المرضي والفحص السريري:
- يستمع الدكتور هطيف بعناية إلى شكاوى المريض، ويسأل عن تاريخ بدء الأعراض، وشدتها، والعوامل التي تزيدها أو تخففها.
- يُجري فحصًا سريريًا دقيقًا للمنطقة المصابة لتقييم الألم، والتورم، ونطاق حركة المفصل، وأي علامات أخرى.
-
التصوير التشخيصي:
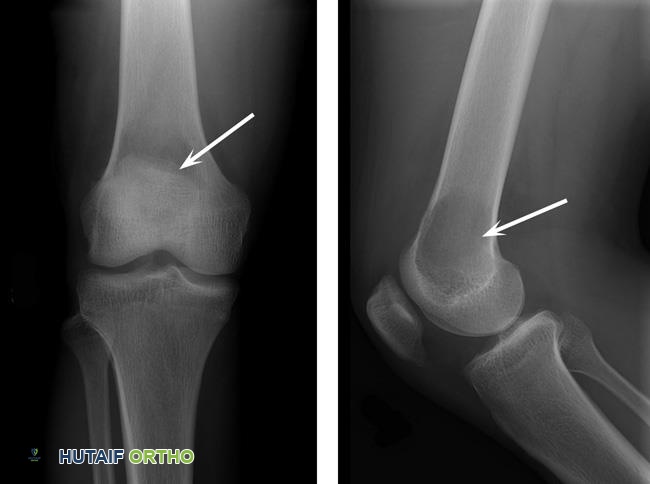
- الأشعة السينية (X-rays): هي الخطوة الأولى في التصوير. تظهر ورم الخلايا العملاقة عادةً كآفة حالّة للعظم (lytic lesion) مع حدود واضحة ولكن غير متصلبة، وقد يكون لها مظهر "فقاعات الصابون" (soap-bubble appearance) بسبب وجود حواجز داخلية.
- التصوير بالرنين المغناطيسي (MRI): يوفر صورًا مفصلة للأنسجة الرخوة والعظم، ويساعد في تحديد مدى انتشار الورم داخل العظم وإلى الأنسجة المحيطة، وتقييم مدى تأثيره على المفصل. كما أنه يكشف عن مستويات السوائل في الورم.
- التصوير المقطعي المحوسب (CT scan): يُستخدم لتقييم تفاصيل القشرة العظمية ومدى تدميرها، وهو مفيد جدًا في التخطيط الجراحي.
- مسح العظام بالنظائر المشعة (Bone Scintigraphy): قد يُستخدم لتقييم نشاط الورم واستبعاد وجود بؤر أخرى (على الرغم من أن الانتشار بعيد نادر جدًا في GCTB).
-
الخزعة (Biopsy):
- تُعد الخزعة ضرورية لتأكيد التشخيص النسيجي لورم الخلايا العملاقة.
- الخزعة بالإبرة (Needle Biopsy): تُجرى عادة تحت توجيه الأشعة (CT أو Fluoroscopy) لأخذ عينة صغيرة من الورم.
- الخزعة المفتوحة (Open Biopsy): قد تكون ضرورية في بعض الحالات للحصول على عينة أكبر.
- يؤكد الدكتور هطيف على أهمية إجراء الخزعة بواسطة جراح ذي خبرة لتجنب تلوث الأنسجة المحيطة، وتحليلها بواسطة أخصائي أمراض نسيجية متخصص في أورام العظام لضمان التشخيص الصحيح.
-
التشخيص التفريقي:
- من المهم التفريق بين ورم الخلايا العملاقة وأورام العظام الأخرى التي قد تبدو متشابهة في التصوير أو الأعراض، مثل: الكيس العظمي المتمدد (Aneurysmal Bone Cyst)، الورم الغضروفي الحميد (Chondroblastoma)، أو حتى بعض الأورام الخبيثة. الخبرة التشخيصية للدكتور هطيف تضمن التمييز الدقيق بين هذه الحالات.
تصنيف ورم الخلايا العملاقة نظام كامباناشي
يُستخدم نظام كامباناشي على نطاق واسع لتصنيف ورم الخلايا العملاقة بناءً على مظهره الإشعاعي ومدى تدميره للعظم، وهو يساعد في توجيه خيارات العلاج:
- الدرجة الأولى (Latent): آفة داخل نخاع العظم، لها حدود واضحة، وقشرة عظمية سليمة.
- الدرجة الثانية (Active): آفة داخل نخاع العظم، توسع في القشرة العظمية مع ترققها، لكنها لا تزال سليمة.
- الدرجة الثالثة (Aggressive): آفة خارج قشرة العظم، مع اختراق للأنسجة الرخوة المحيطة، أو كسر مرضي، أو تدمير كامل للعظم.
يُعد تحديد درجة الورم أمرًا بالغ الأهمية لتخطيط العلاج المناسب وتقييم مخاطر التكرار.
خيارات العلاج الشاملة خبرة الأستاذ الدكتور محمد هطيف
يتطلب علاج ورم الخلايا العملاقة في العظم نهجًا متعدد التخصصات، ويُعد الأستاذ الدكتور محمد هطيف رائدًا في تقديم هذه الرعاية المتكاملة. الهدف الأساسي من العلاج هو استئصال الورم بالكامل مع الحفاظ على وظيفة الطرف المصاب قدر الإمكان وتقليل مخاطر التكرار.
العلاج الدوائي دينوسوماب Denosumab
يُعد دينوسوماب ثورة في علاج ورم الخلايا العملاقة، خاصة في الحالات التي يصعب فيها الاستئصال الجراحي الكامل، أو في حالات التكرار، أو لتحضير الورم للجراحة.
* آلية العمل: دينوسوماب هو جسم مضاد أحادي النسيلة يستهدف RANKL، مما يمنع تنشيط الخلايا العملاقة المسؤولة عن تدمير العظم. يؤدي ذلك إلى تقليل حجم الورم وتقليل نشاطه وتصلب حدوده، مما يسهل الجراحة ويقلل من خطر التكرار.
* دواعي الاستعمال:
* الأورام غير القابلة للاستئصال جراحيًا.
* الأورام المتكررة.
* علاج مساعد قبل الجراحة لتقليل حجم الورم وتصلب حدوده.
* المرضى الذين لا يستطيعون الخضوع للجراحة.
* إشراف الأستاذ الدكتور هطيف: يحدد الدكتور هطيف بدقة متى يكون دينوسوماب هو الخيار الأنسب، ويُشرف على جرعاته ومتابعة المريض لضمان أقصى فائدة بأقل آثار جانبية محتملة.
العلاج الجراحي حجر الزاوية
يُعد التدخل الجراحي هو العلاج الأساسي لمعظم حالات ورم الخلايا العملاقة. يختار الأستاذ الدكتور هطيف الإجراء الأنسب بناءً على حجم الورم، موقعه، درجته، ومدى تدميره للعظم.
الكشط مع العلاجات المساعدة Adjuvant Therapy
هذا هو الإجراء الجراحي الأكثر شيوعًا، ويهدف إلى إزالة الورم من داخل العظم مع الحفاظ على بنية العظم والمفصل.
* العملية: يتم فتح العظم والوصول إلى الورم، ثم يتم كشط الورم بعناية باستخدام أدوات خاصة (curettes).
* العلاجات المساعدة (Adjuvants): لتقليل خطر التكرار، يستخدم الدكتور هطيف علاجات مساعدة داخل التجويف بعد الكشط:
* كي التجويف (High-speed burr): استخدام أداة حفر عالية السرعة لإزالة أي خلايا ورمية متبقية من جدران التجويف.
* الفينول (Phenol): مادة كيميائية تُستخدم لقتل الخلايا الورمية المتبقية.
* النيتروجين السائل (Cryosurgery): تجميد التجويف بالنيتروجين السائل لقتل الخلايا.
* الكي الحراري (Argon beam coagulation): استخدام شعاع الأرجون لكي الخلايا.
* ملء التجويف: بعد الكشط والعلاجات المساعدة، يُملأ التجويف الناتج بـ:
* الأسمنت العظمي (Bone Cement - PMMA): يُفضل الأسمنت العظمي لأنه يوفر دعمًا هيكليًا فوريًا، ويطلق حرارة تساعد في قتل الخلايا الورمية المتبقية، ويسهل اكتشاف أي تكرار مستقبلي في الأشعة.
* الطعوم العظمية (Bone Grafts): سواء كانت ذاتية (من جسم المريض) أو خيفية (من متبرع)، تُستخدم لإعادة بناء العظم، لكنها قد تكون أضعف من الأسمنت العظمي وتزيد من خطر التكرار بسبب عدم وجود تأثير حراري قاتل للخلايا.
* خبرة الأستاذ الدكتور هطيف: يستخدم الدكتور هطيف خبرته الطويلة في تحديد أفضل توليفة من العلاجات المساعدة ومواد ملء التجويف لضمان أفضل النتائج وتقليل معدل التكرار، مع التركيز على الحفاظ على وظيفة المفصل.
الاستئصال الكتلي En Bloc Resection
في بعض الحالات، قد يكون الورم كبيرًا جدًا، أو عدوانيًا للغاية، أو قد تكرر عدة مرات، مما يستدعي إزالة قطعة كاملة من العظم تحتوي على الورم.
* دواعي الاستعمال:
* الأورام الكبيرة التي تسببت في تدمير واسع للعظم.
* الأورام التي اخترقت القشرة العظمية وانتشرت إلى الأنسجة الرخوة المحيطة.
* الكسور المرضية الكبيرة.
* التكرار المتعدد للورم بعد الكشط.
* إعادة البناء: بعد الاستئصال، يجب إعادة بناء الجزء المفقود من العظم والمفصل، وتشمل الخيارات:
* المفاصل الاصطناعية (Endoprosthesis): استبدال الجزء المفقود بمفصل اصطناعي، خاصة في المفاصل الكبيرة مثل الركبة أو الكتف.
* الطعوم العظمية الخيفية (Allograft): استخدام عظم من متبرع لإعادة بناء المنطقة.
* الطعوم العظمية الذاتية (Autograft): استخدام عظم من جزء آخر من جسم المريض.
* مهارة الأستاذ الدكتور هطيف: تتميز جراحات الاستئصال وإعادة البناء بالتعقيد الشديد وتتطلب مهارة جراحية عالية وخبرة واسعة. يستخدم الأستاذ الدكتور محمد هطيف أحدث التقنيات الجراحية لضمان الدقة في الاستئصال وإعادة البناء الفعالة، مما يتيح للمريض استعادة وظيفة الطرف قدر الإمكان.
البتر Amputation
يُعد البتر خيارًا نادرًا جدًا ويُستخدم فقط في الحالات القصوى التي يكون فيها الورم قد دمر الطرف بشكل لا يمكن إصلاحه، أو في حالة العدوى الشديدة التي لا تستجيب للعلاج، أو إذا كانت حياة المريض مهددة.
العلاج الإشعاعي
يُعد العلاج الإشعاعي خيارًا ثانويًا لورم الخلايا العملاقة بسبب المخاطر المحتملة (مثل التحول الخبيث للورم)، ولكنه قد يُستخدم في حالات معينة:
* دواعي الاستعمال:
* الأورام غير القابلة للاستئصال جراحيًا (مثل أورام العمود الفقري أو الحوض التي يصعب الوصول إليها).
* الورم المتكرر الذي لا يمكن علاجه جراحيًا.
* العلاج التلطيفي لتخفيف الألم في الحالات المتقدمة.
* مخاطر: يُناقش الأستاذ الدكتور هطيف بعناية مخاطر وفوائد العلاج الإشعاعي مع المريض، مع التركيز على خطر التحول إلى ساركوما (ورم خبيث) على المدى الطويل، وإن كان ذلك نادرًا.
جدول 2: مقارنة بين خيارات العلاج الجراحي لورم الخلايا العملاقة
| الميزة | الكشط مع العلاجات المساعدة | الاستئصال الكتلي (En Bloc Resection) |
|---|---|---|
| دواعي الاستعمال | معظم الحالات، أورام الدرجة 1 و 2 | أورام كبيرة، عدوانية، متكررة، كسور مرضية |
| الحفاظ على العظم | ممتاز، يُحافظ على معظم بنية العظم | إزالة جزء كبير من العظم، يتطلب إعادة بناء |
| معدل التكرار | أعلى نسبيًا (20-50%)، لكن يقل مع المساعدات | أقل نسبيًا (أقل من 10-15%) |
| مدة التعافي | أقصر نسبيًا | أطول وأكثر تعقيدًا |
| التأثير الوظيفي | جيد جدًا غالبًا، استعادة وظيفة سريعة | قد يتطلب فترة طويلة لإعادة التأهيل، قد تكون الوظيفة محدودة |
| التعقيد الجراحي | أقل تعقيدًا | عالي التعقيد، يتطلب مهارة عالية |
الإجراء الجراحي خطوة بخطوة الكشط مع الأسمنت العظمي كمثال
لتقديم فهم أوضح للمرضى، نشرح هنا إجراء الكشط مع ملء التجويف بالأسمنت العظمي، وهو أحد الإجراءات الأكثر شيوعًا التي يجريها الأستاذ الدكتور محمد هطيف.
التخطيط قبل الجراحة Pre-operative Planning
- التقييم الشامل: يُجري الدكتور هطيف تقييمًا شاملاً باستخدام الأشعة السينية، الرنين المغناطيسي، والتصوير المقطعي لتحديد الحجم الدقيق للورم، موقعه، ومدى تدميره للعظم.
- مناقشة الخيارات: يشرح الدكتور هطيف للمريض وأسرته الخطة الجراحية المقترحة، والمخاطر، والفوائد، والنتائج المتوقعة، والإجابة على جميع استفساراتهم بشفافية تامة.
- الفحوصات الروتينية: تُجرى فحوصات الدم، تخطيط القلب، وفحص الصدر بالأشعة السينية للتأكد من جاهزية المريض للجراحة.
التخدير
- يُعطى المريض تخديرًا عامًا أو موضعيًا (مثل التخدير النصفي) بواسطة فريق تخدير متخصص لضمان راحة المريض وسلامته طوال فترة الجراحة.
الشق الجراحي Incision
- يُجري الأستاذ الدكتور هطيف شقًا جراحيًا دقيقًا ومناسبًا فوق موقع الورم، مع مراعاة الوصول الأمثل للورم وتقليل التأثير الجمالي.
الوصول إلى الورم وكشطه Curettage
- يتم فتح العظم (corticotomy) للوصول إلى التجويف الذي يحتوي على الورم.
- باستخدام أدوات كشط متخصصة، يقوم الدكتور هطيف بإزالة جميع الأنسجة الورمية المرئية بعناية فائقة، مع التأكد من الوصول إلى جميع زوايا التجويف.
تطبيق العلاجات المساعدة Adjuvant Application
- بعد الكشط الأولي، يُستخدم الكي بالكي الكهربائي (high-speed burr) لإزالة أي خلايا مجهرية متبقية على جدران التجويف العظمي.
- بعد ذلك، قد يطبق الدكتور هطيف الفينول أو النيتروجين السائل (حسب الحالة) لتعقيم التجويف وقتل الخلايا الورمية المتبقية. تُغسل المنطقة جيدًا بعد استخدام هذه المواد.
ملء التجويف Cavity Filling
- يُملأ التجويف الناتج بالأسمنت العظمي (PMMA). يُجهز الأسمنت في غرفة العمليات ويوضع في التجويف حيث يتصلب بسرعة، مما يوفر دعمًا هيكليًا فوريًا للعظم ويساعد على قتل الخلايا المتبقية بفعل الحرارة المنبعثة.
الإغلاق Closure
- بعد التأكد من استقرار الأسمنت وتوقف النزيف، يتم إغلاق الشق الجراحي طبقة بعد طبقة، وتُوضع ضمادة معقمة.
الرعاية الفورية بعد الجراحة Immediate Post-operative Care
- يُنقل المريض إلى غرفة الإفاقة للمراقبة الدقيقة
آلام العظام والمفاصل وتقييد حركتها ليس قدراً محتوماً! التشخيص الدقيق والعلاج المتخصص يمكن أن يعيد لك كامل وظيفتك وحريتك في الحركة. لا تدع الألم يسيطر على حياتك.
للحصول على استشارة دقيقة وخطة علاجية مخصصة لحالتك، تواصل فوراً مع مركز الأستاذ الدكتور محمد هطيف:
الأستاذ الدكتور محمد هطيف - أفضل دكتور عظام في صنعاء، وخبير في جراحات العظام والمفاصل والعمود الفقري.. نلتزم بإعادتك لحياة خالية من الألم وحركة طبيعية.
