التهاب العظام المزمن دليلك الشامل للأعراض والتشخيص وطرق العلاج الجراحي
الخلاصة الطبية
التهاب العظام المزمن هو عدوى بكتيرية عميقة ومعقدة تصيب نسيج العظم، وتؤدي إلى تكون نسيج عظمي ميت محاط بغلاف ندبي يمنع وصول المضادات الحيوية. يعتمد العلاج الفعال بشكل أساسي على الاستئصال الجراحي الجذري للأنسجة المصابة، متبوعاً بتقنيات إعادة بناء العظم واستخدام المضادات الحيوية الموجهة.
الخلاصة الطبية السريعة: التهاب العظام المزمن هو عدوى بكتيرية عميقة ومعقدة تصيب نسيج العظم، وتؤدي إلى تكون نسيج عظمي ميت محاط بغلاف ندبي يمنع وصول المضادات الحيوية. يعتمد العلاج الفعال بشكل أساسي على الاستئصال الجراحي الجذري للأنسجة المصابة، متبوعاً بتقنيات إعادة بناء العظم واستخدام المضادات الحيوية الموجهة.
مقدمة شاملة عن التهاب العظام المزمن
يُعد التهاب العظام المزمن، والمعروف طبياً باسم التهاب العظم والنقي المزمن، واحداً من أكثر التحديات الطبية تعقيداً في مجال جراحة العظام. بالنسبة للعديد من المرضى، تمثل هذه الحالة رحلة طويلة ومحبطة، حيث قد تتراجع الأعراض الحادة للعدوى لفترات، لكن البكتيريا تظل كامنة داخل البنية العظمية العميقة.
غالباً ما يعاني المرضى من نوبات تفاقم حادة ومتقطعة قد تمتد لسنوات أو حتى عقود. وعلى الرغم من أن هذه النوبات قد تستجيب مؤقتاً للراحة واستخدام المضادات الحيوية المثبطة، إلا أن القضاء التام على العدوى يتطلب فهماً دقيقاً لطبيعة المرض وتدخلاً جراحياً متخصصاً. تم تصميم هذا الدليل الشامل ليكون المرجع الطبي الأوثق باللغة العربية، ليضع بين يديك كل ما تحتاج لمعرفته حول طبيعة المرض، وكيفية تشخيصه بدقة، والخيارات الجراحية المتقدمة المتاحة للشفاء التام بإذن الله.
طبيعة المرض والتغيرات البيولوجية في العظم
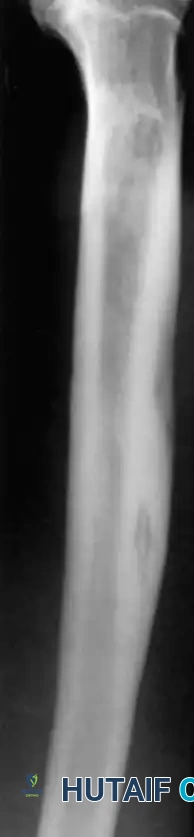
لفهم سبب صعوبة علاج التهاب العظام المزمن، يجب أن نفهم ما يحدث داخل العظم المصاب. السمة الفسيولوجية الأساسية لهذا المرض هي وجود ما يُعرف بـ "العظم الميت" أو الشظية العظمية الميتة، والتي تكون محتجزة داخل غلاف من الأنسجة الرخوة المتضررة بشدة.
هذه البؤر العظمية المصابة بالعدوى تُحاط عادة بغلاف من العظم المتصلب وضعيف التروية الدموية، والذي يُحاط بدوره بغشاء عظمي سميك، وعضلات متندبة، وأنسجة ليفية تحت الجلد.

هذا الغلاف الندبي الخالي من الأوعية الدموية يخلق حاجزاً فسيولوجياً يجعل المضادات الحيوية التي تؤخذ عن طريق الفم أو الوريد غير فعالة تقريباً، حيث لا تستطيع الأدوية اختراق هذا الحاجز للوصول إلى البكتيريا.
بالإضافة إلى ذلك، تقوم البكتيريا في حالات التهاب العظام المزمن بتغيير سلوكها، حيث تتحول من حالة حرة ونشطة إلى حالة مستقرة، وتشكل ما يُعرف بـ "الغشاء الحيوي البكتيري". هذا الغشاء اللزج يحمي البكتيريا من خلايا المناعة في الجسم ويمنع اختراق الأدوية المضادة للميكروبات. لذلك، فإن الاستئصال الجراحي الجذري مع العلاج الدوائي الموجه هو السبيل الوحيد للشفاء.
أنظمة تصنيف التهاب العظام المزمن
يتطلب علاج التهاب العظام المزمن نهجاً منظماً لتحديد ما إذا كان العلاج يجب أن يكون بسيطاً أم معقداً، وهل الهدف هو الشفاء التام أم التخفيف من الأعراض. يُعد نظام تصنيف سيرني ومادر المعيار الذهبي عالمياً في هذا المجال، حيث يجمع بين مدى انتشار المرض في العظم والحالة الصحية العامة للمريض.
أنواع الإصابة التشريحية
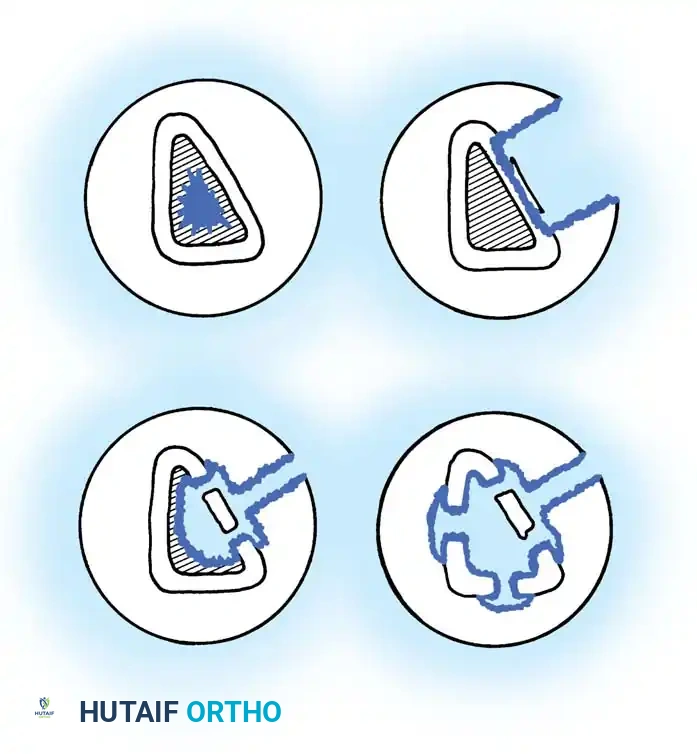
تُقسم الإصابة من الناحية التشريحية إلى أربعة أنواع رئيسية تحدد مدى تضرر نسيج العظم
- النوع الأول الإصابة النخاعية يقتصر المرض على التجويف الداخلي للعظم، ويُشاهد عادة في حالات العدوى المنتقلة عبر الدم أو بعد التهاب المسامير النخاعية المستخدمة في تثبيت الكسور.
- النوع الثاني الإصابة السطحية تقتصر العدوى على السطح الخارجي للعظم، وتحدث غالباً نتيجة فقدان الأنسجة الرخوة المغطية للعظم بسبب الحوادث أو الإصابات.
- النوع الثالث الإصابة الموضعية آفة مستقرة ومحددة جيداً تتميز بوجود تجويف وعظم ميت يشمل كامل سماكة القشرة العظمية. إزالة هذا الجزء جراحياً لا تؤثر على الاستقرار الميكانيكي للعظم.
- النوع الرابع الإصابة المنتشرة آفة ممتدة تسبب عدم استقرار ميكانيكي في العظم، سواء كان هذا الضعف موجوداً وقت التشخيص أو حدث نتيجة الاستئصال الجراحي الضروري لتنظيف العدوى.
الحالة الصحية والفسيولوجية للمريض
لا يعتمد نجاح العلاج على العظم فقط، بل على قدرة جسم المريض على الشفاء، وتُصنف إلى
| فئة المريض | الوصف الطبي | القدرة على التعافي |
|---|---|---|
| الفئة أ | مريض يتمتع بمناعة طبيعية، وتروية دموية ممتازة، وصحة عامة جيدة. | استجابة ممتازة للعلاجات الجراحية المعقدة. |
| الفئة ب | مريض يعاني من مشاكل صحية. قد تكون موضعية مثل ضعف الأوردة أو الشرايين، أو جهازية مثل السكري، سوء التغذية، التدخين، أو ضعف المناعة. | يحتاج إلى تحسين حالته الصحية (مثل ضبط السكر والإقلاع عن التدخين) قبل أي تدخل جراحي معقد. |
| الفئة ج | مريض حالته الصحية حرجة جداً، حيث تفوق مخاطر الجراحة الفوائد المرجوة منها. | يُفضل التركيز على الرعاية التلطيفية أو قد يُنصح بالبتر في الحالات القصوى لإنقاذ حياة المريض. |
الأسباب وعوامل الخطر المؤدية للمرض
لا يحدث التهاب العظام المزمن من فراغ، بل هو نتيجة لتطور عدوى لم يتم القضاء عليها بشكل كامل في مراحلها الأولى. تتعدد الأسباب والطرق التي تصل بها البكتيريا إلى العظم، ومن أهمها
مصادر العدوى الرئيسية
- التعرض لإصابات وحوادث شديدة الكسور المفتوحة التي يخترق فيها العظم الجلد تسمح للبكتيريا بالدخول المباشر إلى نسيج العظم.
- العمليات الجراحية السابقة جراحات تثبيت الكسور باستخدام الشرائح والمسامير قد تكون عرضة للعدوى إذا لم تلتئم الجروح بشكل سليم.
- الانتشار عبر الدم قد تنتقل بكتيريا من التهاب في مكان آخر في الجسم (مثل التهاب المسالك البولية أو التهاب الرئة) عبر مجرى الدم لتستقر في العظم.
- الانتشار من أنسجة مجاورة القرح الجلدية العميقة، خاصة في القدم السكرية، يمكن أن تمتد وتصل إلى العظام المجاورة.
عوامل تزيد من خطر الإصابة
- مرض السكري يؤدي إلى ضعف الدورة الدموية وتلف الأعصاب، مما يقلل من قدرة الجسم على محاربة العدوى واكتشاف الجروح مبكراً.
- التدخين يقلل بشكل كبير من تدفق الدم إلى الأنسجة والعظام، مما يعيق عملية الشفاء ويزيد من خطر فشل العمليات الجراحية.
- ضعف الجهاز المناعي المرضى الذين يتلقون علاجات كيماوية، أو أدوية مثبطة للمناعة، أو يعانون من أمراض مناعية.
- أمراض الأوعية الدموية تمنع وصول الأكسجين والخلايا المناعية والمضادات الحيوية إلى منطقة العدوى.
الأعراض والعلامات السريرية للمرض
يتميز التهاب العظام المزمن بأعراض قد تظهر وتختفي على فترات متباعدة. من الضروري الانتباه لهذه العلامات ومراجعة الطبيب المختص فور ظهورها
- ألم مستمر أو متقطع في العظم ألم عميق يزداد سوءاً مع الحركة أو الضغط على المنطقة المصابة، وقد يوقظ المريض من النوم.
- تكون النواصير الجلدية ظهور فتحات صغيرة على الجلد (نواصير) تفرز صديداً أو سوائل بشكل متكرر. هذه النواصير قد تُغلق لفترة ثم تفتح مجدداً عندما يزداد الضغط داخل العظم.
- تورم واحمرار موضعي انتفاخ في الأنسجة المحيطة بالعظم المصاب مع ارتفاع في حرارة الجلد الموضعي.
- تصلب المفاصل المجاورة صعوبة في تحريك المفصل القريب من منطقة العدوى بسبب الألم والتورم.
- أعراض عامة نادرة على عكس الالتهاب الحاد، نادراً ما يعاني مريض الالتهاب المزمن من حمى شديدة أو قشعريرة، إلا في حالات التفاقم الحاد للعدوى.
طرق التشخيص الدقيقة والحديثة
يعتمد تشخيص التهاب العظام المزمن على دمج الفحص السريري الدقيق، والتحاليل المخبرية، والتصوير الطبي المتقدم، وصولاً إلى التقييم النسيجي والميكروبيولوجي النهائي.
الفحص السريري والتحاليل المخبرية
يقوم طبيب العظام بفحص دقيق لسلامة الجلد والأنسجة الرخوة، وتحديد مناطق الألم، وتقييم استقرار العظم، وفحص الحالة العصبية والدموية للطرف المصاب.
أما بالنسبة للتحاليل المخبرية، فهي غالباً غير محددة. في حين أن مؤشرات الالتهاب مثل سرعة ترسب الدم والبروتين التفاعلي ترتفع لدى معظم المرضى، إلا أن عدد كريات الدم البيضاء يرتفع في حوالي 35% فقط من الحالات.
تقنيات التصوير الطبي المتقدمة
لا توجد تقنية تصوير واحدة يمكنها تأكيد أو استبعاد المرض بشكل مطلق، لذلك يُعد النهج المتعدد الوسائط ضرورياً للتخطيط الجراحي.
- الأشعة السينية العادية هي الفحص الأولي الأساسي. ظهور علامات مثل هشاشة العظام الموضعية، تدمير القشرة العظمية، وتواجد العظم الميت، يشير بقوة إلى التشخيص.
- تصوير الناسور الملون إذا كان هناك ناسور نشط يفرز صديداً، يتم حقن مادة ملونة لتتبع مسار الناسور وتحديد بؤرة العدوى العميقة، مما يساعد الجراح في التخطيط للعملية.
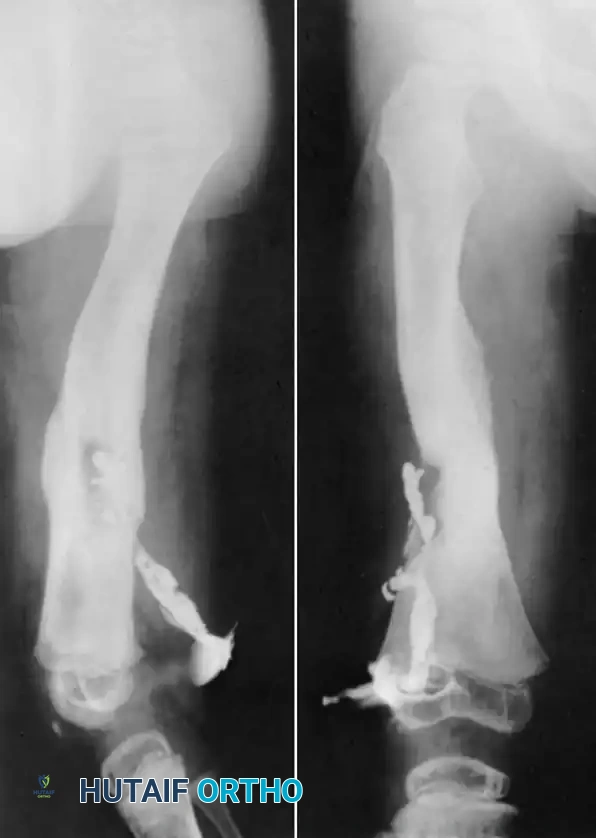
- التصوير المقطعي المحوسب يوفر دقة لا مثيل لها في إظهار بنية العظم القشري. وهو الأفضل لتحديد الشظايا العظمية الميتة الصغيرة وتخطيط المدى الهندسي للاستئصال العظمي.
- التصوير بالرنين المغناطيسي الخيار الأفضل لتقييم مدى انتشار العدوى في نخاع العظم وتورم الأنسجة الرخوة المحيطة.
- الطب النووي تستخدم فحوصات مثل المسح بعنصر التكنيتيوم أو الجاليوم أو الكريات البيضاء الموسومة لتحديد نشاط العدوى، خاصة في حالات القدم السكرية.
الخزعة العميقة للعظم
يُعد أخذ خزعة عظمية عميقة مفتوحة وإرسالها للتحليل النسيجي والزراعة البكتيرية (الهوائية واللاهوائية والفطرية) هو "المعيار الذهبي" للتشخيص. يجب تجنب أخذ مسحات سطحية من النواصير لأنها مضللة جداً ولا تعكس نوع البكتيريا الحقيقية الموجودة في عمق العظم.
المبادئ الأساسية للعلاج الجراحي
يجب أن يدرك المريض أن المضادات الحيوية وحدها لا يمكنها القضاء على التهاب العظام المزمن بسبب انعدام التروية الدموية في العظم الميت ووجود الغشاء البكتيري الواقي. حجر الزاوية في العلاج هو التنظيف والاستئصال الجراحي الجذري، لتحويل البيئة الميتة والمصابة إلى بيئة حيوية غنية بالتروية الدموية.
إن عدم إزالة الأنسجة المصابة بالكامل هو السبب الرئيسي لعودة المرض. أثبتت الدراسات الطبية أن الاستئصال الواسع (ترك هامش أمان أكثر من 5 ملم من العظم السليم) يؤدي إلى نسبة نجاح تقارب 100%، بينما الاستئصال غير الكافي يؤدي إلى انتكاسات متكررة.
خطوات العملية الجراحية لتنظيف العظم
تُعد جراحة استئصال العظم الميت والتنظيف الجذري عملية دقيقة وتتطلب تخطيطاً مسبقاً ومهارة عالية من جراح العظام.
التحضير والتخطيط قبل الجراحة
يتم حقن النواصير بمادة ملونة (أزرق الميثيلين) قبل الجراحة بـ 24 ساعة. هذا الإجراء يصبغ الأنسجة المتليفة والمصابة، مما يجعل من السهل على الجراح التعرف عليها واستئصالها ككتلة واحدة بالكامل.
الخطوات الجراحية التفصيلية
- الوصول الجراحي واستئصال الناسور يقوم الجراح بعمل شق جراحي واسع واستئصال جميع النواصير المصبوغة وصولاً إلى العظم.
- إزالة الغشاء العظمي يتم فتح الغشاء العظمي السميك والمصاب لكشف العظم المتصلب تحته.
- فتح نافذة عظمية باستخدام أدوات جراحية دقيقة، يتم فتح نافذة في قشرة العظم للوصول إلى التجويف الداخلي الذي يحتوي على الخراج أو العظم الميت.
- التنظيف الجذري العميق تُزال جميع الشظايا الميتة، والصديد، والأنسجة النخاعية المريضة. يستمر الجراح في التنظيف حتى يصل إلى نسيج عظمي سليم ينزف دماً صحياً (ما يُعرف بعلامة البابريكا).
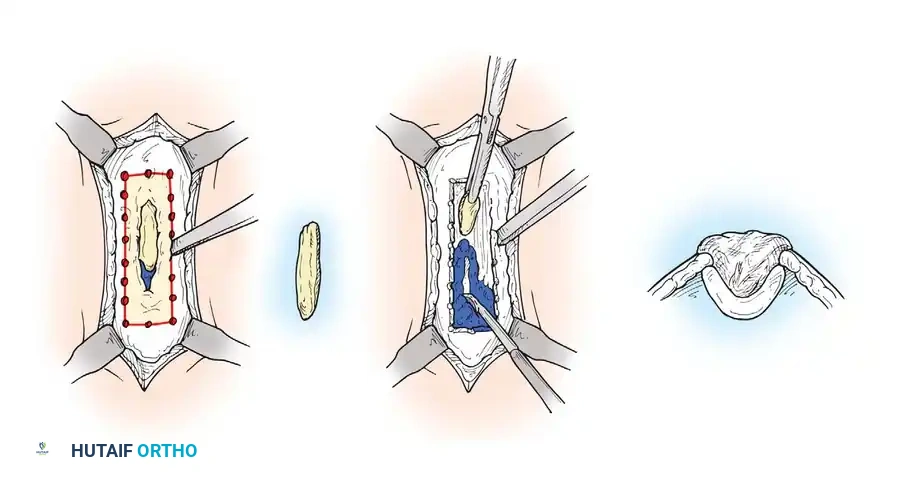
- تشكيل الفجوة العظمية بعد إزالة العدوى، يتم تنعيم حواف العظم لمنع تكون زوايا حادة قد تتجمع فيها السوائل وتسبب عدوى جديدة.
- تثبيت العظم إذا أدى التنظيف إلى إضعاف العظم ميكانيكياً، يجب تثبيته. يُفضل استخدام المثبت الخارجي الدائري (مثل جهاز إليزاروف) لأنه يوفر ثباتاً ممتازاً دون وضع مسامير معدنية داخل المنطقة المصابة بالعدوى.
إدارة الفراغ العظمي وتقنيات إعادة البناء
بعد التنظيف الجذري، يتبقى فراغ كبير في العظم. إذا تُرك هذا الفراغ دون إدارة طبية صحيحة، سيمتلئ بالدم المتخثر ويصبح بيئة مثالية لعودة البكتيريا. لذلك، يستخدم جراحو العظام تقنيات متقدمة لملء هذا الفراغ وإعادة بناء الطرف.
استخدام حبيبات المضادات الحيوية الموضعية
يتم استخدام حبيبات مصنوعة من مادة خاصة (PMMA) مشبعة بجرعات عالية جداً من المضادات الحيوية المقاومة للحرارة. هذه الحبيبات تؤدي وظيفتين ملء الفراغ العظمي فيزيائياً، وتوفير تركيز هائل من المضادات الحيوية موضعياً (غالباً 100 ضعف التركيز في الدم) دون التسبب في آثار جانبية على الكلى أو الكبد.
تُربط هذه الحبيبات عادة بخيط جراحي لتسهيل إزالتها لاحقاً. يتم إغلاق الجرح جزئياً أو تغطيته بغشاء خاص لخلق بيئة مغلقة عالية التركيز الدوائي. تُزال هذه الحبيبات بعد 3 إلى 6 أسابيع ليتم بعدها إجراء الترقيع العظمي النهائي.
تقنية الترقيع العظمي المفتوح
تعتمد هذه التقنية على مبدأ أن الأنسجة الحبيبية الغنية بالأوعية الدموية والعظام الإسفنجية الذاتية تتمتع بمقاومة طبيعية للعدوى.
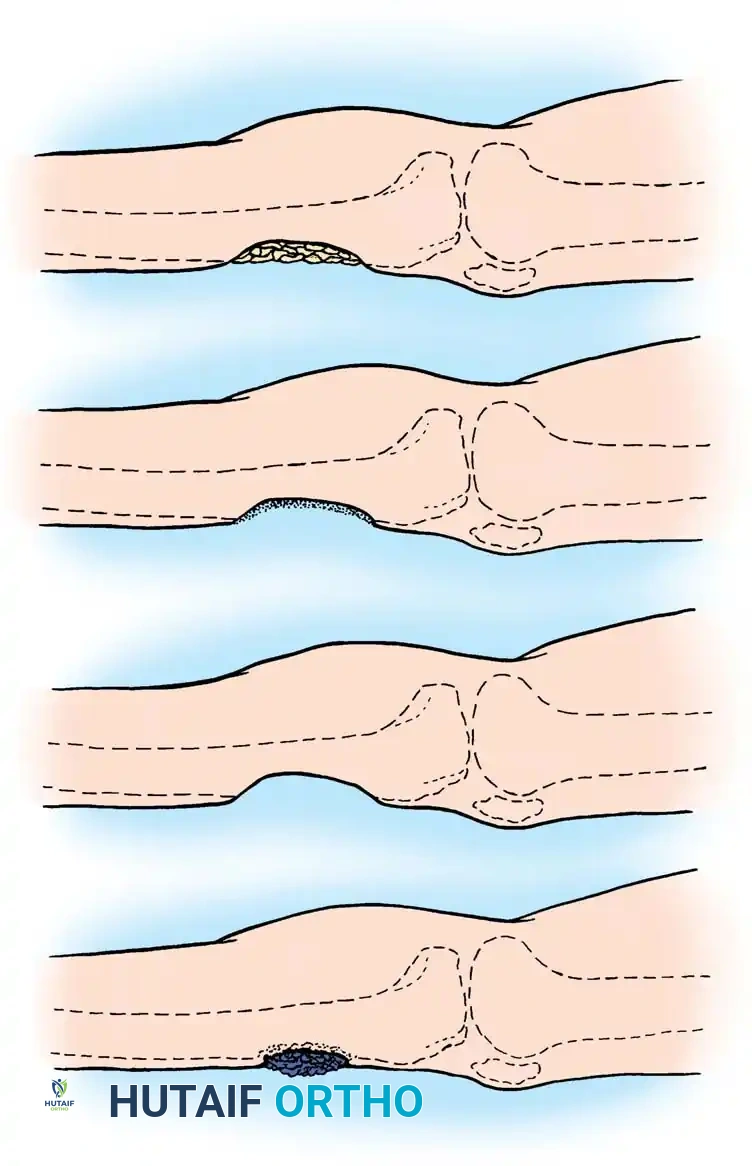
* المرحلة الأولى التنظيف الجذري وترك الجرح مفتوحاً حتى تتكون طبقة صحية من الأنسجة الحبيبية.
* المرحلة الثانية يتم حشو الفراغ بكثافة باستخدام عظم إسفنجي يؤخذ عادة من حوض المريض.
* المرحلة الثالثة يُترك العظم المزروع ليلتئم تدريجياً أو يُغطى برقعة جلدية بمجرد أن تكسوه الأنسجة الحيوية بالكامل.
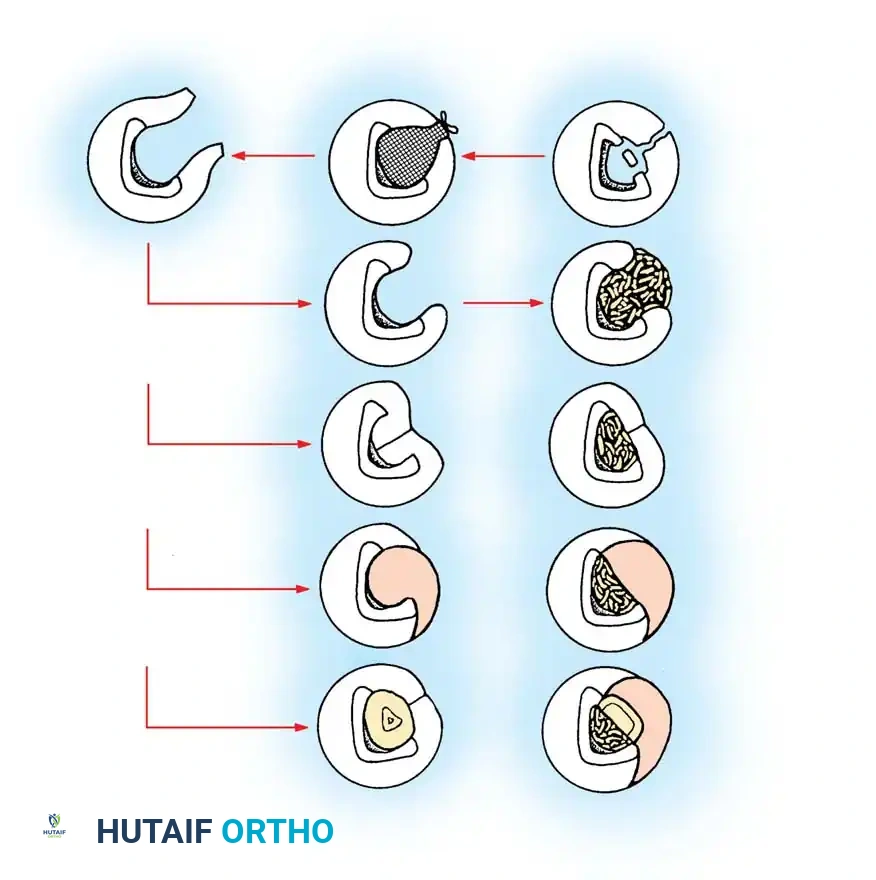
نقل الأنسجة العضلية والسدائل
عندما يكون الجلد والأنسجة المحيطة بالعظم متضررة بشدة، يجب جلب أنسجة حيوية جديدة لتغطية العظم وتحسين التروية الدموية. يمكن استخدام عضلات من نفس الساق (مثل عضلة السمانة) وتدويرها لتغطية الجرح، أو في حالات الفراغات الكبيرة، يتم الاستعانة بجراح التجميل المجهري لنقل عضلة من الظهر أو البطن مع أوعيتها الدموية وربطها مجهرياً في الساق. هذه العضلة الجديدة تجلب دماً غنياً بالأكسجين والمضادات الحيوية إلى المنطقة المريضة.
تطويل العظام وإعادة البناء بجهاز إليزاروف
في حالات الفقدان العظمي الواسع جداً، يتم اللجوء إلى تقنية التطويل العظمي. يتم استئصال كامل الجزء المصاب من العظم، ثم يُستخدم جهاز التثبيت الخارجي الدائري (إليزاروف) لقطع العظم السليم في منطقة أخرى وسحبه تدريجياً (بمعدل 1 ملم يومياً) لملء الفراغ. هذه التقنية المعجزة تسمح بنمو عظم جديد وصحي تماماً، مما يعالج العدوى ويعوض النقص العظمي في آن واحد.
بروتوكول التعافي وما بعد الجراحة
لا تنتهي رحلة العلاج بانتهاء العملية الجراحية، بل تُعد مرحلة ما بعد الجراحة حاسمة لضمان عدم عودة المرض.
العلاج بالمضادات الحيوية
يُعد تحديد مدة ونوع المضادات الحيوية أمراً بالغ الأهمية ويتم بالتعاون مع طبيب مختص في الأمراض المعدية. تقليدياً، يتلقى المريض مضادات حيوية عن طريق الوريد لمدة 6 أسابيع بناءً على نتيجة الزراعة البكتيرية. حديثاً، تدعم الأبحاث الطبية إمكانية التحول إلى مضادات حيوية قوية عن طريق الفم بعد فترة قصيرة من العلاج الوريدي، بشرط التزام المريض التام بالجرعات.
التأهيل والمتابعة الطبية
- تثبيت وحماية الطرف يجب حماية العظم المعالج باستخدام الجبائر أو المثبت الخارجي لمنع حدوث كسور مرضية في منطقة الجراحة التي تكون ضعيفة مؤقتاً.
- التحميل والمشي يُمنع المريض من تحميل وزنه الكامل على الطرف المصاب حتى تظهر الأشعة السينية التئاماً تاماً للترقيع العظمي أو العظم الجديد.
- المراقبة طويلة الأمد يحتاج المرضى إلى متابعة مستمرة لسنوات، تشمل تحاليل الدم الدورية وصور الأشعة، حيث أن العدوى قد تعود بعد سنوات من الشفاء الظاهري، مما يتطلب يقظة دائمة من المريض والطبيب.
الأسئلة الشائعة حول التهاب العظام المزمن
هل يمكن الشفاء تماما من التهاب العظام المزمن
نعم، الشفاء التام ممكن بإذن الله، ولكنه يتطلب تدخلاً جراحياً جذرياً لاستئصال جميع الأنسجة الميتة والمصابة، متبوعاً ببروتوكول صارم من المضادات الحيوية الموجهة. العلاج الدوائي وحده دون جراحة نادراً ما يحقق الشفاء التام في الحالات المزمنة.
لماذا لا تستجيب العدوى للمضادات الحيوية العادية
لا تستجيب العدوى لأن البكتيريا تختبئ داخل نسيج عظمي ميت لا تصله الدورة الدموية، وبالتالي لا يصل إليه الدواء. كما أن البكتيريا تفرز غشاءً حيوياً لزجاً يحميها من الأدوية ومن جهاز مناعة الجسم.
كم تستغرق فترة العلاج والتعافي بعد الجراحة
تختلف فترة التعافي بشكل كبير حسب شدة الحالة وحجم الفراغ العظمي. في الحالات المتوسطة قد يستغرق التعافي من 3 إلى 6 أشهر، بينما في الحالات المعقدة التي تتطلب استخدام جهاز إليزاروف لتطويل العظم، قد تمتد فترة العلاج من عام إلى عامين.
هل البتر هو الحل النهائي لالتهاب العظام
البتر ليس الخيار الأول ويُعتبر الملاذ الأخير. يُلجأ إليه فقط في الحالات التي تهدد فيها العدوى حياة المريض (تسمم الدم)، أو عندما يكون الطرف مشوهاً ومؤلماً لدرجة تجعله غير وظيفي، أو إذا كانت الحالة الصحية للمريض لا تتحمل العمليات الجراحية الترميمية الطويلة.
ما هو دور التغذية في علاج التهاب العظام
التغذية السليمة تلعب دوراً محورياً في بناء نسيج عظمي جديد والتئام الجروح. يحتاج المريض إلى كميات كافية من البروتينات، والفيتامينات (خاصة فيتامين سي ودال)، والمعادن مثل الكالسيوم والزنك لدعم جهاز المناعة وتسريع عملية الشفاء.
هل يؤثر التدخين على نجاح العملية الجراحية
نعم، وبشكل خطير جداً. النيكوتين يسبب انقباض الأوعية الدموية الدقيقة، مما يقلل من وصول الدم والأكسجين والمضادات الحيوية إلى العظم المصاب. يُشترط التوقف التام عن التدخين بأسابيع قبل وبعد الجراحة لضمان نجاح الترقيع العظمي والتئام الجروح.
ما هي علامات انتكاس المرض وعودة العدوى
يجب الانتباه لعودة الألم الموضعي، ظهور تورم أو احمرار جديد، انفتاح جرح قديم، أو خروج إفرازات وصديد من الجلد. ظهور أي من هذه العلامات يستدعي مراجعة طبيب العظام فوراً.
هل يمكن تركيب مفاصل صناعية لمريض يعاني من التهاب عظام مزمن
لا يُنصح بتركيب أي أجزاء معدنية أو مفاصل صناعية في منطقة تعاني من عدوى نشطة. يجب القضاء على العدوى تماماً والتأكد من خلو المنطقة من البكتيريا لعدة أشهر أو سنوات قبل التفكير في أي جراحة لتبديل المفاصل.
ما هو جهاز إليزاروف ولماذا يستخدم في هذه الحالات
جهاز إليزاروف هو مثبت خارجي حلقي يُثبت في العظم بواسطة أسلاك دقيقة. يُستخدم لتثبيت العظم بعد إزالة الأجزاء المصابة، ويسمح بتطويل العظم السليم تدريجياً لتعويض النقص العظمي الناتج عن الاستئصال الجراحي.
هل مرض السكري يمنع إجراء العملية الجراحية
مرض السكري لا يمنع الجراحة، ولكنه يتطلب تحضيراً خاصاً. يجب التحكم الدقيق في مستويات السكر في الدم قبل وأثناء وبعد الجراحة لضمان التئام الجروح وتقليل خطر فشل العملية، حيث أن السكر المرتفع يضعف مناعة الجسم بشكل كبير.

